- TIẾNG VIỆT
- TIẾNG ANH
- TOÁN PHỔ THÔNG
- TOÁN LOGIC
- TOÁN SỐ LIỆU
- VẬT LÝ
- HÓA HỌC
- NGUYÊN TỬ
- BẢNG TUẦN HOÀN NGUYÊN TỐ HÓA HỌC
- TỐC ĐỘ PHẢN ỨNG
- CÂN BẰNG HÓA HỌC
- ĐIỆN LI
- ĐIỆN PHÂN
- LIÊN KẾT HÓA HỌC
- PHẢN ỨNG HÓA HỌC
- HÓA HỌC VÔ CƠ
- HÓA HỌC HỮU CƠ
- SINH HỌC
- ĐỊA LÍ
- LỊCH SỬ
ESTE
I. KHÁI NIỆM - ĐỒNG PHÂN - DANH PHÁP
1. KHÁI NIỆM
Khi THAY THẾ nhóm OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm OR’ thì được ESTE.
VD: Cho axit axetic tác dụng với ancol etylic (xúc tác H2SO4 đặc, t0)
CH3-COOH + C2H5-OH CH3COOC2H5 + H2O
TỔNG QUÁT
R-COOH + R'-OH RCOOR' + H2O
- CTCT của este ĐƠN CHỨC: RCOOR’
R : gốc hiđrocacbon của axit hoặc H.
R’: gốc hiđrocacbon của ancol (R # H)
- CTCT chung của este NO ĐƠN CHỨC:
CnH2n+1COOCmH2m+1 (n ≥ 0, m ≥ 1)
CxH2xO2 (x ≥ 2)
2. ĐỒNG PHÂN
-Ứng với công thức CnH2nO2 có thể có các loại đồng phân mạch hở sau:
+ Axit no, đơn chức, mạch hở (số đồng phân: 2n-3 với n < hoặc = 5)
+ Este no, đơn chức, mạch hở (số đồng phân: 2n-2 với n < hoặc = 4)
+ Andehit – ancol
+ Xeton – ancol
+ Andehit – ete
+ Xeton – ete
VD ứng với CTPT C4H8O2 có các đồng phân este sau:
HCOOCH2-CH2-CH3: n-propyl fomat
HCOOCH-(CH3)2: isopropyl fomat
CH3COOC2H5: etyl axetat
C2H5COOCH3: metyl propionat
3. DANH PHÁP
- TÊN GỌI: Tên gốc hiđrocacbon của ancol + tên gốc axit.
- Tên GỐC AXIT: Xuất phát từ tên của axit tương ứng, thay đuôi ic → at.
HCOO- : Fomat
CH3COO- : Axetat
CH3-CH2COO- : Propionat
CH2=CHCOO- : Acrylat
CH2=C(CH3)COO-: Metacrylat
C6H5COO- : Benzoat
VD. CH3COOCH2CH2CH3: propyl axetat
HCOOCH3: metyl fomat
- Tên GỐC HIDROCACBON
CH3 – : Metyl
C2H5 – : Etyl
CH3-CH2-CH2 – : Propyl
(CH3)2CH- : Isopropyl
C6H5– : Phenyl
C6H5CH2– : Benzyl
CH2=CH- : Vinyl
CH2=CH-CH2– : Anlyl
II. TÍNH CHẤT VẬT LÍ
- Các este là chất LỎNG hoặc chất RẮN trong điều kiện THƯỜNG,Ít tan hoặc không tan trong nước.
- Có nhiệt độ sôi THẤP HƠN hẳn so với các axit ĐỒNG PHÂN hoặc các ancol có cùng khối lượng mol phân tử hoặc có cùng số nguyên tử cacbon.
VD
|
CH3CH2CH2COOH (M = 88) Tan nhiều trong nước |
CH3[CH2]3CH2OH (M = 88), Tan ít trong nước |
CH3COOC2H5 (M = 88), Không tan trong nước |
* NGUYÊN NHÂN
Giữa các phân tử este KHÔNG tạo được liên kết hiđro với nhau và liên kết hiđro giữa các phân tử este với nước RẤT KÉM.
- Các este thường có MÙI ĐẶC TRƯNG:
isoamyl axetat có mùi CHUỐI CHÍN
etyl butirat và etyl propionat có mùi DỨA
geranyl axetat có mùi HOA HỒNG…
III.TÍNH CHẤT HOÁ HỌC
1. PHẢN ỨNG THUỶ PHÂN
- Phản ứng thực hiện trong môi trường axit loãng và được đun nóng
RCOOR’ + H2O RCOOH + R’OH
Este + nước axit cacboxylic + ancol
- Phản ứng xà phòng hóa
RCOOR’ + NaOH → RCOONa + R’OH
Este + dung dịch bazơ → muối + ancol
VD: CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
2. PHẢN ỨNG GỐC HIĐROCACBON
- Este không no (este của axit không no hoặc ancol không no) có khả năng tham gia phản ứng cộng và phản ứng trùng hợp.
Đây là tính chất do liên kết π quy định (tương tự như hiđrocacbon tương ứng)
- Một số phản ứng thuộc loại này có ứng dụng quan trọng là:
-
- Phản ứng chuyển hoá dầu (chất béo lỏng) thành mỡ (chất béo rắn)
(C17H33COO)3C3H5 + 3H2 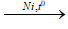
(Triolein) (Tristearin)
-
- Phản ứng trùng hợp vinyl axetat thành poli(vinyl axetat)
-
- Trùng hợp metyl metacrylat thành poli(metyl metacrylat) – thuỷ tinh hữu cơ plexiglas).
-
- Phản ứng tráng gương của este của axit fomic– (xem lại anđehit).
3. PHẢN ỨNG KHỬ ESTE
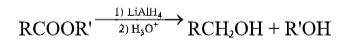
CHÚ Ý: Anhiđrit axit, Halogenua axit cũng bị líti - nhôm hiđrua khử tương tự.
4. MỘT SỔ PHẢN ỨNG THỦY PHÂN ĐẶC BIỆT
Căn cứ vào sơ đồ phản ứng xà phòng hoá hay phản ứng thuỷ phân este ta có thể căn cứ vào sản phẩm tạo thành để suy đoán cấu tạo của este ban đầu.
Không nhất thiết sản phẩm cuối cùng phải có ancol, tuỳ thuộc vào việc nhóm –OH đính vào gốc hiđrocacbon có cấu tạo như thế nào mà sẽ có các phản ứng tiếp theo xảy ra để có sản phẩm cuối cùng hoàn toàn khác nhau, hoặc nữa là do cấu tạo bất thường của este gây nên.
Một số trường hợp thuỷ phân đặc biệt của este (không chứa halogen) thường gặp trong bài toán định lượng là:
- Este + NaOH →1 muối + 1 anđehit
Este đơn chức có gốc ancol dạng công thức R-CH=CH-
RCOOCH=CH2 + NaOH → RCOONa + CH3CHO
VD CH3COOCH=CH-CH3
- Este + NaOH →1 muối + 1 xeton
Este đơn chức với dạng công thức R’ –COO – C(R)=C(R”)R’’’
RCOOC(CH3)=CH2 + NaOH → RCOONa + CH3COCH3
VD CH3-COO-C(CH3)= CH2 tạo axeton khi thuỷ phân.
- Este + NaOH →1 muối + 1 ancol + H2O
Este- axit: HOOC-R-COOR’
- Este + NaOH →2 muối + H2O
RCOOC6H5 + 2NaOH → RCOONa + C6H5ONa + H2O
Este của phenol: C6H5OOC-R
- Este + NaOH →1 muối + anđehit + H2O
Hiđroxi- este: RCOOCH(OH)-R’
- Este + NaOH →1 muối + xeton + H2O
Hiđroxi- este: RCOOC(R)(OH)-R’
(Tham khảo các trường hợp Ancol không bền)
III.ỨNG DỤNG VÀ ĐIỀU CHẾ
1. ỨNG DỤNG
Các este có ứng dụng rộng rãi trong đời sống.
- Làm dung môi.
VD: butyl và amyl axetat được dùng để pha sơn tổng hợp.
- Sản xuất nhiều chất quan trọng như:
poli(metyl acrylat) và poli(metyl metacrylat) dùng làm thủy tinh hữu cơ
poli(vinyl axetat) dùng làm chất dẻo hoặc thủy phân thành poli(vinyl ancol) dùng làm keo dán.
- Một số este của axit phtalic được dùng là chất hóa dẻo, dược phẩm…
- Một số este có mùi thơm hoa quả được dùng trong công nghiệp thực phẩm và mĩ phẩm…
VD. Isoamyl axetat: CH3COOCH2CH2(CH3)2: mùi chuối, dùng trong thực phẩm
Geranyl axetat: CH3COOC10H17: mùi hoa hồng, dùng trong mĩ phẩm…
2. ĐIỀU CHẾ
- Thực hiện phản ứng este hóa giữa ancol và axit
Điều kiện phản ứng: H2SO4 đặc và đun nóng
Vai trò H2SO4 đặc là xúc tác của phản ứng và làm nhiệm vụ hút nước.
- Thực hiện phản ứng cộng giữa axit và hiđrocacbon không no
RCOOH + C2H2 → RCOOCH = CH2
- Thực hiện phản ứng giữa muối Na của axit và dẫn xuất halogen
RCOONa + R’X → RCOOR’ + NaX (xt, t0)
- Thực hiện phản ứng giữa phenol và anhidrit axit
(RCO)2O + C6H5OH → RCOOC6H5 + RCOOH
![Phản ứng trùng hợp Vinyl axetat | vinyl axetat ra poli vinyl axetat | CH3COOCH=CH2 ra [-CH(OOCCH3)-CH2-]n](https://vietjack.com/phan-ung-hoa-hoc/images/phuong-trinh-nch3coochch2-a01.PNG)
![Phản ứng trùng hợp Metyl metacrylat | metyl metacrylat ra poli metyl metacrylat | CH2=C(CH3)-COOCH3 ra [-CH2-C(CH3)(COOCH3)-]n](https://vietjack.com/phan-ung-hoa-hoc/images/phuong-trinh-nch2cch3cooch3-a01.PNG)