CHƯƠNG 5: ANDEHIT XETON
I. ĐỊNH NGHĨA
- Công thức tổng quát của xeton:
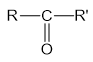
- Trong đó R, R’ là gốc hiđrocacbon có thể giống hoặc khác nhau.
II. TÍNH CHẤT HÓA HỌC
Hai chất này khá giống nhau về tính chất hóa học. Riêng ta chỉ tập trung vào tính chất của Anđêhit
- Andehit vừa có tính oxi hóa vừa có tính khử.
1. TÍNH OXI HÓA
- Tác dụng với hidro (xúc tác Ni, t0)
CH3-CHO + H2 → CH3-CH2-OH
R-CHO + H2 → R-CH2OH
* Tổng quát
R(CHO)x + xH2 → R(CH2OH)x
Andehit + H2 → ancol bậc 1
* LƯU Ý
- Trong phản ứng của anđehit với H2: Nếu gốc R có các liên kết pi thì H2 cộng vào cả các liên kết pi đó.
- Phản ứng với H2 chứng tỏ anđehit có tính oxi hóa.
2. TÍNH KHỬ
- Tác dụng với AgNO3/NH3
- Phản ứng đặc trưng của andehit là phản ứng tráng gương
CH3-CHO + 2AgNO3 + 3NH3 + H2O → CH3-COONH4 + 2NH4NO3 + 2Ag
* Tổng quát
R(CHO)x + 2xAgNO3 + 3xNH3 + xH2O → R(COONH4)x + xNH4NO3 + 2xAg
=> Phản ứng chứng minh anđehit có tính khử và được dùng để nhận biết anđehit.
- Riêng HCHO có phản ứng:
HCHO + 4AgNO3 + 6NH3 + 2H2O → (NH4)2CO3 + 4NH4NO3 + 4Ag
* Lưu ý:
- Phản ứng tổng quát ở trên áp dụng với anđehit không có nối ba nằm đầu mạch. Nếu có nối ba nằm ở đầu mạch thì H của C nối ba cũng bị thay thế bằng Ag.
- Tác dụng với dung dịch brom
- Andehit làm mất màu dung dịch nước brom.
R-CHO + Br2 + H2O → R-COOH + 2HBr.
- Tác dụng với Cu(OH)2/OH-
- Andehit còn tác dụng được với Cu(OH)2 trong môi trường kiềm cho kết tủa Cu2O màu đỏ gạch:
CH3-CH=O + 2Cu(OH)2 + NaOH → CH3-COONa + Cu2O + 3H2O
* Tổng quát:
R(CHO)x + 2xCu(OH)2↓ → R(COOH)x + xCu2O↓ + 2xH2O
=> Phản ứng này được dùng để nhận biết anđehit.
- Riêng đối với HCHO:
HCHO + 4Cu(OH)2 + 2NaOH → Na2CO3 + 2Cu2O + 6H2O
- Tác dụng với oxi (xúc tác Mn2+, t0)
- Andehit có phản ứng oxi hóa bởi O2 tạo ra axit cacboxylic tương ứng với xúc tác Mn2+ và ở nhiệt độ cao:
2CH3-CHO + O2 → 2CH3-COOH
* Tổng quát
R(CHO)x + x/2O2 → R(COOH)x
- Phản ứng cháy
CxHyOz + (x + y/4 - z/2)O2 → xCO2 + y/2H2O
Nếu đốt cháy anđehit mà nCO2 = nH2O thì anđehit thuộc loại no, đơn chức, mạch hở.
CnH2n+1CHO → (n + 1)CO2 + (n + 1)H2O