Dạng 2: TÌM KIM LOẠI
-Tìm 1 kim loại :
- Nếu đề đã cho biết hóa trị của kim loại thì ta chỉ cần tìm khối lượng mol của nó. Trường hợp không tìm được trực tiếp khối lượng mol thì ta tìm giới hạn khối lượng mol.
- Nếu đề chưa cho biết hóa trị của kim loại thì ta tìm giá trị của biểu thức (M là khối lượng mol của kim loại, n là hóa trị của nó). Lần lượt xét các giá trị n= 1; 2; 3 để tìm M.
-Tìm 2 kim loại
- Phương pháp hay được sử dụng là phương pháp trung bình : Thay 2 kim loại bằng 1 kim loại có khối lượng mol trung bình là . Dựa vào giả thiết và tính chất của giá trị trung bình (M1<<M2, M1, M2 là khối lượng mol của hai kim loại) để suy ra hai kim loại.
VÍ DỤ
Cho 1,9 gam hỗn hợp muối cacbonat và hiđrocacbonat của kim loại kiềm M tác dụng hết với dung dịch HCl (dư), sinh ra 0,448 lít khí (ở đktc). Xác định kim loại M.
Công thức muối cacbonat và hiđrocacbonat của kim loại kiềm M là M2CO3 và MHCO3.
Phương trình phản ứng hóa học :
M2CO3 + 2HCl ➞2MCl + CO2 + H2O
MHCO3 + HCl ➞MCl + CO2 + H2O
Theo các phản ứng ta thấy: Tổng số mol hỗn hợp muối = số mol của CO2 = 0,02 mol.
Gọi khối lượng mol trung bình của hai muối là MTB, ta có: M + 61 <MTB < 2M + 60 (*)
Mặt khác MTB= 95 (**)
Kết hợp giữa (*) và (**) 17,5 <MTB< 34 Kim loại M là Na.
VÍ DỤ 2
A là hỗn hợp 2 kim loại kiềm X và Y thuộc 2 chu kì kế tiếp. Nếu cho A tác dụng vừa đủ với dung dịch HCl thì thu được a gam 2 muối, còn nếu cho A tác dụng vừa đủ với dung dịch H2SO4 thì thu được 1,1807a gam 2 muối. Xác định X và Y.
Đặt công thức chung của hai kim loại kiềm là R, khối lượng mol trung bình của chúng là MTB .
Chọn số mol của R tham gia phản ứng là 1 mol.
Phương trình phản ứng :
2R + 2HCl ➜ 2RCl + H2 (1)
mol: 1 1
2R + H2SO4 ➜ R2SO4 + H2 (2)
mol: 1 0,5
Khối lượng của muối clorua là : (MTB+35,5) = a. (3)
Khối lượng muối sunfat là : 0,5.(2MTB+96) =1,1807a. (4)
Từ (3) và (4) ta cóMTB=33,67.
Nhận xét : MNa <MTB< MK => X và Y là Na và K.
VÍ DỤ 3
X là kim loại thuộc phân nhóm chính nhóm II (hay nhóm IIA). Cho 1,7 gam hỗn hợp gồm kim loại X và Zn tác dụng với lượng dư dung dịch HCl, sinh ra 0,672 lít khí H2 (đktc). Mặt khác, khi cho 1,9 gam X tác dụng với lượng dư dung dịch H2SO4 loãng, thì thể tích khí hiđro sinh ra chưa đến 1,12 lít (đktc). Xác định kim loại X.
Đặt công thức chung của hai kim loại X và Zn là R.
Phương trình phản ứng :
R + 2HCl ➜ RCl2 + H2 (1)
mol: 0,03 0,03
Khối lượng mol trung bình của hỗn hợp là :![]()
Phản ứng của X với dung dịch H2SO4 loãng :
X + H2SO4 ➜ XSO4 + H2 (2)
mol: < 0,05 < 0,05
Theo (2) và giả thiết ta suy ra 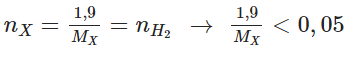
=>MX > 38
Từ (*) và (**) ta suy ra X là Ca.
VÍ DỤ 4
Cho 3,6 gam hỗn hợp X gồm K và một kim loại kiềm M tác dụng vừa hết với nước, thu được 2,24 lít H2 ở 0,5 atm và 0oC. Biết số mol kim loại M trong hỗn hợp lớn hơn 10% tổng số mol 2 kim loại. Xác định kim loại M.
Gọi khối lượng mol trung bình của hai kim loại kiềm là MTB .
Phương trình phản ứng :
2K + 2H2O ➜ 2KOH + H2 (1)
2M + 2H2O ➜ 2MOH + H2 (2)
Theo các phản ứng ta thấy : mol MTB= 36 gam/mol.
Vì MTB< MK nên MTB> MM =>M có thể là Na hoặc Li.
Giả sử trong hỗn hợp M chiếm 10% về số mol, ta có :
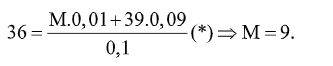
Trên thực tế trong hỗn hợp M chiếm hơn 10% về số mol nên số mol của nó lớn hơn 0,01, số mol K nhỏ hơn 0,09. Vậy từ (*) suy ra M >9 => M là Na.
VÍ DỤ 5
Hòa tan hết 46 gam hỗn hợp gồm Ba và hai kim loại kiềm A, B thuộc hai chu kì kế tiếp vào nước, thu được dung dịch D và 11,2 lít khí đo ở đktc. Nếu thêm 0,18 mol Na2SO4 vào dung dịch D thì dung dịch sau phản ứng vẫn chưa kết tủa hết bari. Nếu thêm 0,21 mol Na2SO4 vào dung dịch D thì dung dịch sau phản ứng còn dư Na2SO4. Xác định tên hai kim loại kiềm.
Gọi kí hiệu chung của hai kim loại kiềm là M, khối lượng mol là
![]() .
.
Gọi số mol trong 46 gam hỗn hợp đầu:
Các phương trình phản ứng:
2M + 2H2O ➜ 2MOH + H2 (1)
mol: a a 0,5a
Ba + 2H2O ➜ Ba(OH)2 + H2 (2)
mol: b b b
Số mol H2 = 0,5 mol nên : 0,5a + b = 0,5 (3)
Khi cho dung dịch thu được tác dụng với dung dịch Na2SO4:
Ba(OH)2 + Na2SO4 ➜ BaSO4 + 2NaOH (4)
Khi thêm 0,18 mol Na2SO4, trong dung dịch còn dư Ba(OH)2 nên b > 0,18.
Khi thêm 0,21 mol Na2SO4, trong dung dịch còn dư Na2SO4 nên b < 0,21.
Mặt khác :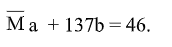 (5)
(5)
Kết hợp (3), (5) ta có :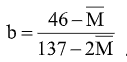 .
.
Mặt khác : 0,18 < b < 0,21
=>29,7 <![]() < 33,34.
< 33,34.
Khối lượng mol trung bình của 2 kim loại kiềm liên tiếp là : 29,7 <![]() < 33,34. Hai kim loại đó là Na (Na = 23) và K ( K = 39).
< 33,34. Hai kim loại đó là Na (Na = 23) và K ( K = 39).